فهرست عناوین
- مقدمه
- هویت شیمیایی و ویژگی های کلیدی اسید استیک
- شکل ها و غلظت ها: اسید استیک گلاسیال در برابر محلول های رقیق
- گریدهای خلوص و کنترل کیفیت در آزمایشگاه های دانشگاهی
- تهیه ی بافر: بافرهای استات برای pH حدود 3.6 تا 5.6
- تنظیم pH و متوقف کردن واکنش ها در آزمایشگاه های مرطوب
- کاربردها در سنتز آلی و شیمی مواد
- کروماتوگرافی و علم جداسازی: HPLC، TLC و الکتروفورز مویینه
- ملاحظات طیف سنجی و سازگاری با دستگاه ها
- بافت شناسی و سلول شناسی: فیکساسیون، رنگ آمیزی و دکلسیفیکاسیون
- زیست مولکولی: اسیدهای نوکلئیک و پروتئین ها
- میکروبیولوژی و کشت سلول: محیط، استریلیتی و متابولیسم
- نگهداری نمونه، استخراج و پیش تغلیظ
- ایمنی، کاربری و مدیریت ریسک اسید استیک
نوشته شده توسط شرکت صنایع استیک ایران
منتشر شده توسط شرکت صنایع استیک ایران
تاریخ انتشار مقاله : 26-09-1404
تاریخ بروزرسانی مقاله : 26-09-1404
تعداد کلمات : 3300
آدرس مقاله : لینک مقاله
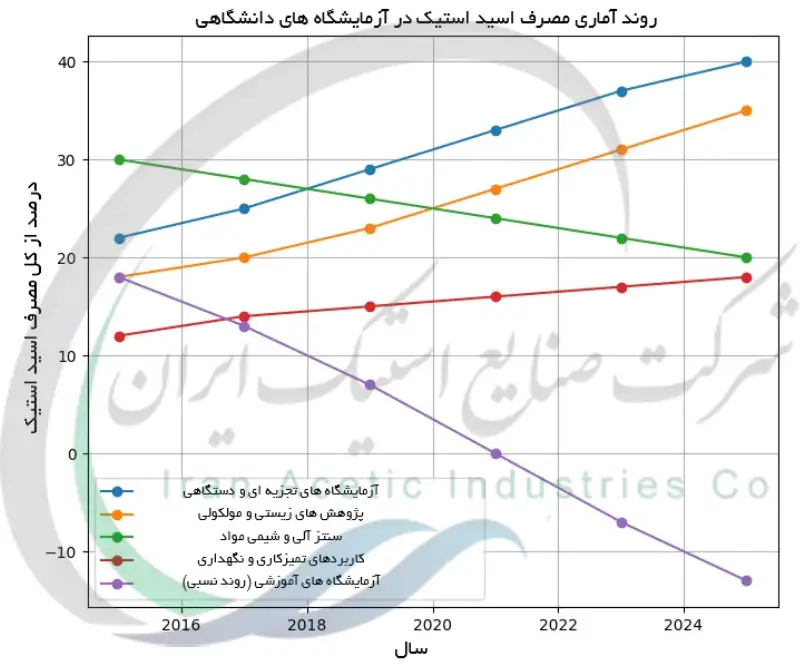
مصرف اسید استیک در آزمایشگاه ها و تحقیقات دانشگاهی

مقدمه
اسید استیک یکی از همه کاره ترین مواد شیمیایی در آزمایشگاه های مدرن هستند و به دلیل اسیدیته ی متعادل، سازگاری با حلال های مختلف، و رفتار قابل پیش بینی در شرایط گوناگون بسیار پرکاربرد است. در پژوهش دانشگاهی، این ماده در کارهای روزمره مثل تهیه ی بافر، تنظیم pH، بهینه سازی فاز متحرک در کروماتوگرافی، و آماده سازی نمونه برای تحلیل های زیستی و شیمیایی دیده می شود. پژوهشگران همچنین در بافت شناسی و سلول شناسی، در روش های زیست مولکولی مرتبط با نمک های استات، و در شیمی مواد که اسیدیته ی کنترل شده می تواند روی تبلور، شیمی سطح، یا رفتار پلیمر اثر بگذارد از آن استفاده می کنند. چون اسید استیک هم به صورت مایع غلیظ (معروف به اسید استیک گلاسیال) و هم به شکل محلول های رقیق قابل استفاده است، از کلاس های آموزشی تا سامانه های تحلیلی پیشرفته کاربرد دارد و به همین دلیل در فرآیند تامین مواد آزمایشگاهی، عباراتی مانند خرید اسید استیک شازند گالن 20 لیتری معمولا در فهرست سفارش مراکز آموزشی و تحقیقاتی دیده می شود. با این حال، خورندگی و بوی تند آن نیازمند ایمنی دقیق، نگهداری درست و مدیریت مسئولانه ی پسماند است تا افراد، دستگاه ها و کیفیت داده های پژوهشی محافظت شوند.
هویت شیمیایی و ویژگی های کلیدی اسید استیک
اسید استیک (اتانوئیک اسید) یک اسید آلی کوچک است که هم به عنوان دهنده ی پروتون و هم به عنوان منبع یون استات عمل می کند و به همین دلیل برای کاربرد اسید استیک در آزمایشگاه و پژوهش دانشگاهی بسیار مفید است. ساختار مولکولی آن امکان پیوند هیدروژنی قوی را فراهم می کند و همین موضوع توضیح می دهد چرا با آب و بسیاری از حلال های آلی قطبی به خوبی مخلوط می شود. به عنوان یک اسید ضعیف، راهی قابل کنترل برای تغییر pH می دهد و در بسیاری از موارد نسبت به اسیدهای معدنی قوی تغییرات ناگهانی کمتری ایجاد می کند؛ این ویژگی برای کار با زیست مولکول های حساس به pH یا کمپلکس های فلزی اهمیت دارد. بوی مشخص آن می تواند نشانه ی آزاد شدن بخار باشد، اما همین موضوع نشان می دهد تهویه در کار روزمره ضروری است. یک نکته ی فیزیکی مهم این است که اسید استیک بسیار غلیظ می تواند در دماهای نزدیک به محیط جامد شود، بنابراین گاهی در انبارها حالت کریستالی موقت دیده می شود. در توسعه ی روش ها، اسیدیته ی متوسط آن به ایجاد شرایط یونی تکرارپذیر کمک می کند و در شیمی تهیه، در تشکیل نمک و برخی واکنش ها نقش دارد. مجموع این ویژگی ها باعث شده اسید استیک در آزمایشگاه یک نیاز ثابت در محیط های آموزشی و پژوهشی باشد.
شکل ها و غلظت ها: اسید استیک گلاسیال در برابر محلول های رقیق
در آزمایشگاه ها معمولا اسید استیک در دو شکل کاربردی استفاده می شود: اسید استیک گلاسیال (بسیار غلیظ) و محلول های آبی رقیق که برای پروتکل های مشخص آماده می شوند. اسید استیک گلاسیال زمانی انتخاب می شود که یک محلول مادر قوی برای رقیق سازی دقیق لازم باشد، یا زمانی که مقدار آب باید حداقل باشد، یا وقتی واکنش به محیط آلی اسیدی نیاز دارد. در مقابل، محلول های رقیق اسید استیک برای تنظیم pH، مراحل رنگ آمیزی، شستشو، و اسیدی کردن ملایم نمونه ها رایج هستند. غلظت اهمیت زیادی دارد چون خطرات، فراریت، و رفتار شیمیایی با افزایش قدرت تغییر می کند: اسید استیک غلیظ بخار آزار دهنده ی بیشتری آزاد می کند و می تواند سوختگی شدید ایجاد کند، در حالی که محلول رقیق ایمن تر است اما همچنان نیاز به رعایت اصول دارد. برای تکرارپذیری، برچسب گذاری دقیق شامل غلظت، تاریخ، و کاربرد (مثل «0.1 تا 1 درصد برای افزودنی کروماتوگرافی» یا «0.1 مولار برای بافر استات») بسیار کمک کننده است. رقیق سازی درست هم مهم است چون افزودن سریع اسید غلیظ می تواند گرما و نواحی با pH بسیار پایین ایجاد کند و به مواد حساس آسیب بزند.
گریدهای خلوص و کنترل کیفیت در آزمایشگاه های دانشگاهی
انتخاب گرید مناسب یک عامل پنهان اما بسیار اثرگذار در کاربرد اسید استیک در آزمایشگاه و پژوهش دانشگاهی است. در آزمایشگاه های آموزشی، گریدهای عمومی برای تیتر کردن یا تهیه ی بافر کافی است، اما در شیمی تجزیه و روش های حساس، گریدهای با خلوص بالاتر مورد نیاز است تا آلودگی های جذب کننده ی UV، فلزات کم مقدار، و باقی مانده های غیر فرار به حداقل برسند. در کروماتوگرافی و به ویژه روش های همراه با طیف سنجی جرمی، حتی ناخالصی های کوچک می توانند نویز زمینه را بالا ببرند، خط مبنا را تغییر دهند، یا پیک های مزاحم ایجاد کنند؛ بنابراین اسید استیک بخشی از طراحی روش محسوب می شود نه فقط یک حلال معمولی. در پژوهش های زیستی نیز کیفیت می تواند روی آزمون های آنزیمی و مراحل کار با اسیدهای نوکلئیک اثر بگذارد و یون های ناخواسته یا مواد آلی باقی مانده ممکن است مراحل بعدی را مهار کند. کنترل کیفیت عملی می تواند شامل اجرای بلانک در روش های تحلیلی، توجه به تغییر بوی غیر معمول به عنوان نشانه ی آلودگی، و استفاده از ظروف و پمپ های اختصاصی برای کاهش آلودگی متقاطع باشد. استانداردسازی انتخاب گرید در سطح یک گروه یا دانشکده نیز تکرارپذیری بین آزمایشگاه ها را بهتر می کند، مخصوصا در مراکز خدماتی مشترک.
تهیه ی بافر: بافرهای استات برای pH حدود 3.6 تا 5.6
بافرهای استات که از اسید استیک و یک نمک استات (معمولا سدیم استات) ساخته می شوند بسیار پرکاربرد هستند، چون در محدوده ی اسیدی ملایم پایداری خوبی ایجاد می کنند و بسیاری از روش های بیوشیمی و تحلیل به این بازه نیاز دارند. در پژوهش دانشگاهی، بافر استات در آزمون های آنزیمی، مراحل کار با پروتئین، و برخی روش های کروماتوگرافی کمک می کند تا pH کنترل شود و رفتار اتصال و شستشو قابل پیش بینی باشد. طراحی بافر معمولا بر نسبت اسید به باز مزدوج تکیه دارد و امکان هدف گیری pH را با دقت مناسب فراهم می کند، در حالی که قدرت یونی هم قابل کنترل می ماند. دما، غلظت، و حضور مواد همزمان می تواند pH اندازه گیری شده را تغییر دهد، بنابراین بسیاری از آزمایشگاه ها شرایط تهیه را استاندارد می کنند و در پروتکل ها ثبت می کنند تا تکرارپذیری حفظ شود. یک مزیت دیگر این است که بافرهای استات معمولا از محلول های مادر رایج به سادگی تهیه می شوند و در صورت ورود به سیستم های زیستی می توانند فیلتر شوند. در نمونه های دارای فلز، پژوهشگران خطر کمپلکس شدن یا رسوب را هم در نظر می گیرند و در صورت نیاز غلظت را تنظیم می کنند. در مجموع، تهیه ی بافر استات یکی از اصلی ترین دلایل حضور اسید استیک در فهرست مواد مصرفی آزمایشگاه ها است.
تنظیم pH و متوقف کردن واکنش ها در آزمایشگاه های مرطوب
اسید استیک یک ابزار قابل کنترل برای تنظیم pH و متوقف کردن واکنش ها است، به ویژه زمانی که پژوهشگر یک اسید ملایم می خواهد که بتواند آن را کم کم و با دقت اضافه کند. در کار روزمره، این ماده می تواند محلول های قلیایی را به بازه ی pH هدف برساند، پایداری برخی آنالیت ها را که در pH بالا تخریب می شوند افزایش دهد، یا واکنش های کاتالیز شده با باز را با تغییر دسترسی پروتون متوقف کند. در روش های بیوشیمی، اسیدی کردن حساب شده می تواند فعالیت آنزیم را کاهش دهد، واکنش های جانبی ناخواسته را کم کند، یا به مراحل رسوب دهی و جداسازی فاز که به حالت بار مولکول ها وابسته هستند کمک کند. برای نتیجه ی یکنواخت، اسید استیک معمولا قطره ای اضافه می شود و همزدن کامل انجام می گیرد، سپس pH بعد از رسیدن به تعادل دوباره بررسی می شود تا بیش از حد تنظیم نشود. در کار با ماکرومولکول های حساس، روش افزودن به اندازه ی pH نهایی مهم است، چون نواحی موضعی با اسیدیته ی بالا می تواند پروتئین را دناتوره کند یا به اسیدهای نوکلئیک آسیب بزند اگر اختلاط کافی نباشد. بسیاری از پژوهشگران اسید استیک را زمانی انتخاب می کنند که می خواهند کنترل مناسب بر اسیدیته داشته باشند و در عین حال آلودگی یونی مزمن کمتری نسبت به برخی اسیدهای معدنی ایجاد شود.
کاربردها در سنتز آلی و شیمی مواد
در شیمی دانشگاهی، اسید استیک نقش های گوناگونی در سنتز آلی و پژوهش های مرتبط با مواد دارد و بسته به سیستم می تواند حلال، کاتالیزور ملایم، یا شرکت کننده ی واکنش باشد. اسیدیته ی آن از تبدیل های کلاسیک مثل تشکیل استر پشتیبانی می کند و در شرایط اسیدی می تواند به پیش بردن تعادل کمک کند. در شیمی کمپلکس ها و مواد، مقدار کنترل شده ی اسید استیک می تواند روی جوانه زنی، رشد بلور، و شیمی سطح اثر بگذارد؛ به همین دلیل در برخی سنتزهای مواد متخلخل، کمپلکس های فلزی، و فرمولاسیون نانوذرات دیده می شود. امتزاج پذیری آن با آب امکان تنظیم تدریجی قطبیت و اسیدیته ی محیط را فراهم می کند، که برای آزمایش هایی مفید است که تغییرات کوچک روی مورفولوژی یا بازده اثر چشمگیر دارد. همچنین در برخی شرایط، شیمی استات برای تشکیل نمک های فلزی درجا به کار می رود و این نمک ها می توانند پیش ماده یا منبع فلز محلول باشند؛ همین منطق علمی، پیوند مستقیمی با کاربرد اسید استیک در صنایع الکترونیک و باتری دارد که در آن کنترل دقیق شیمی محلول و تشکیل گونه های فلزی اهمیت بالایی دارد. چون مقدار آب رفتار سیستم را به شدت تغییر می دهد، آزمایشگاه ها معمولا مشخص می کنند که از اسید استیک گلاسیال استفاده می کنند یا محلول آبی، و شرایط دقیق را ثبت می کنند تا تکرارپذیری در پروژه های دانشجویی و خروجی های پژوهشی حفظ شود.
کروماتوگرافی و علم جداسازی: HPLC، TLC و الکتروفورز مویینه
اسید استیک در علم جداسازی یک افزودنی کلیدی است، چون مقدارهای کوچک آن می تواند شکل پیک را بهتر کند، یونیزاسیون را مدیریت کند، و برهمکنش های ناخواسته را در تحلیل کاهش دهد. کاربرد آن در کروماتوگرافی گسترش یافته اند چون پژوهشگران اسیدیته ی قابل تنظیم می خواهند بدون این که نمک های غیر فرار و ماندگار وارد سیستم کنند. در کروماتوگرافی مایع، درصدهای پایین اسید استیک می تواند pH فاز متحرک را تنظیم کند، دنباله دار شدن پیک برای ترکیبات بازی را کم کند، و رفتار نگهداشت را پایدارتر سازد. در روش های همراه با طیف سنجی جرمی، گاهی اسید استیک برای کمک به پروتونه شدن انتخاب می شود، در حالی که شرایط همچنان با یونیزاسیون و تمیزی دستگاه سازگار می ماند. در TLC، اسید استیک گاهی در مخلوط حلال توسعه دهنده استفاده می شود تا قطبیت تنظیم شود و جذب خیلی قوی کاهش یابد، مخصوصا وقتی ترکیب در شرایط خنثی دچار کشیدگی لکه می شود. در الکتروفورز مویینه و روش های مشابه، اسید استیک و سامانه های استات می توانند بخشی از طراحی الکترولیت زمینه باشند و رسانایی و pH را کنترل کنند. چون روش های جداسازی به تغییرات کوچک حساس هستند، استانداردسازی غلظت، ترتیب اختلاط، و گرید حلال برای تکرارپذیری ضروری است.
ملاحظات طیف سنجی و سازگاری با دستگاه ها
فراتر از جداسازی، اسید استیک می تواند به شکل ظریف اما مهم روی طیف سنجی و تصمیم های سازگاری با دستگاه اثر بگذارد. در UV Vis، پژوهشگران در نظر می گیرند که محلول های اسید استیک و استات می توانند در طول موج های بسیار پایین روی خط مبنا اثر بگذارند، بنابراین انتخاب بلانک و یکسان بودن ترکیب حلال برای کار کمی اهمیت دارد. در IR، سیگنال های قوی گروه های عاملی اسید استیک می تواند در پایش واکنش مفید باشد، اما اگر به عنوان حلال یا افزودنی استفاده شود ممکن است با پیک های هدف همپوشانی ایجاد کند. در NMR، اسید استیک می تواند به عنوان جزء باقی مانده در نمونه یا بخشی از بافر حضور داشته باشد، پس تفسیر دقیق و آماده سازی یکنواخت کمک می کند اشتباه در انتساب رخ ندهد. سازگاری با دستگاه هم موضوعی عملی است: اگرچه اسید استیک معمولا از اسیدهای معدنی قوی ملایم تر است، محلول های غلیظ هنوز می توانند به برخی فلزات آسیب بزنند، چسب ها را تضعیف کنند، و بعضی پلاستیک ها را در تماس طولانی تحت فشار قرار دهند. به همین دلیل پژوهشگران غلظت و زمان تماس را با مسیر سیال و مواد سازنده هماهنگ می کنند و شستشوهای کنترل شده انجام می دهند. این جزئیات به حفظ قابلیت اعتماد داده ها و کاهش خرابی دستگاه در محیط های دانشگاهی کمک می کند.
بافت شناسی و سلول شناسی: فیکساسیون، رنگ آمیزی و دکلسیفیکاسیون
اسید استیک در بافت شناسی و سلول شناسی شناخته شده است، چون می تواند روی مورفولوژی سلول، جزئیات هسته، و کیفیت رنگ آمیزی اثر بگذارد اگر با دقت استفاده شود. در برخی سامانه های فیکساسیون، اسید استیک برای تقویت حفظ ساختار هسته و بهتر شدن مشاهده ی کروماتین به کار می رود و این موضوع در آموزش و پژوهش میکروسکوپی مهم است. همچنین در برخی روش های رنگ آمیزی، مقدار کم آن به عنوان اسیدی کننده استفاده می شود تا کنتراست بهتر شود، اتصال رنگ تنظیم شود، یا تفکیک ساختارهای بافتی دقیق تر انجام گیرد. در بعضی رویکردهای دکلسیفیکاسیون، اسیدهای ضعیف زمانی انتخاب می شوند که پژوهشگر یک فرایند ملایم تر می خواهد که یکپارچگی ساختاری و سازگاری با رنگ آمیزی های بعدی حفظ شود، هرچند سرعت و کنترل نقطه ی پایان همچنان اهمیت دارد. در برخی آماده سازی های سلول شناسی نیز مراحل کنترل شده ی اسید استیک برای شفاف سازی، کاهش زمینه، یا لیز کنترل شده در آماده سازی های تخصصی استفاده می شود. چون این کارها به زمان، غلظت، و دما حساس هستند، استانداردسازی دستورها و مستندسازی روشن برای هر نمونه ضروری است. با رعایت ایمنی و تهویه ی مناسب، اسید استیک به تولید لام های یکنواخت و نتایج تصویربرداری قابل مقایسه در گروه های پژوهشی کمک می کند.
زیست مولکولی: اسیدهای نوکلئیک و پروتئین ها
اسید استیک در زیست مولکولی هم به طور مستقیم و هم از طریق سامانه های مبتنی بر استات نقش دارد و این سامانه ها در کار با اسیدهای نوکلئیک و پروتئین ها بسیار رایج هستند. یک نمونه ی مهم، استفاده ی گسترده از نمک های استات در رسوب دهی اسیدهای نوکلئیک است؛ جایی که شیمی استات در حضور الکل به تجمع DNA یا RNA کمک می کند و بازده بازیابی را بالا می برد و برخی ناخالصی ها را کاهش می دهد. اسید استیک همچنین در ساخت بافرها دیده می شود، به ویژه در سامانه های تریس استات که در الکتروفورز و کارهای روتین زیست مولکولی استفاده می شوند و یون استات رسانایی و رفتار pH را شکل می دهد. در کار با پروتئین ها، اسیدی کردن کنترل شده با اسید استیک می تواند روی حلالیت اثر بگذارد، به رسوب انتخابی کمک کند، یا برخی برهمکنش های غیر کووالانسی را در پاکسازی نمونه کاهش دهد، البته پژوهشگران از شرایط خیلی سخت که دناتوراسیون برگشت ناپذیر ایجاد کند پرهیز می کنند. چون آنزیم ها و آزمون های آشکارسازی به اسیدیته ی باقی مانده یا قدرت یونی حساس هستند، آزمایشگاه ها معمولا تایید می کنند که خنثی سازی یا تعویض بافر به اندازه ی کافی انجام شده است. در محیط دانشگاهی، کاربرد اسید استیک در زیست مولکولی بیشتر یک مجموعه نقش انعطاف پذیر است تا یک پروتکل واحد.
میکروبیولوژی و کشت سلول: محیط، استریلیتی و متابولیسم
در میکروبیولوژی و کشت سلول، اسید استیک با دقت استفاده می شود چون هم ابزار تنظیم pH است و هم می تواند یک عامل تنش زیستی باشد. در سطح پایین و کنترل شده، می تواند به تنظیم pH محیط کمک کند یا شرایط استات تعریف شده برای مطالعه ی متابولیسم میکروبی، رفتار تخمیر، یا پاسخ های تنشی ایجاد کند. برخی پروژه های دانشگاهی از مواجهه با اسید استیک به عنوان مدل تنش اسیدی در مخمر و باکتری استفاده می کنند تا انتقال غشایی، تنظیم pH درون سلولی، و سازگاری ژنی بررسی شود. با این حال، چون اسید استیک در غلظت های بالاتر رشد را مهار می کند یا به سلول آسیب می زند، راهبرد دوزدهی و ظرفیت بافری باید برنامه ریزی و ثبت شود. در کشت سلول پستانداران، افزودن کنترل نشده مناسب نیست چون افت موضعی pH می تواند به سلول آسیب بزند حتی اگر pH نهایی حجم کلی قابل قبول به نظر برسد. استریلیتی و نحوه ی آماده سازی نیز مهم است: محلول ها باید با تکنیک تمیز تهیه شوند و در صورت ورود به سیستم های حساس ممکن است فیلتراسیون انجام شود. در مجموع، اسید استیک در پژوهش های میکروبیولوژی و کشت سلول کاربردهای زیادی دارد، اما به مدیریت دقیق متغیرهای شیمیایی و زیستی نیاز دارد.
نگهداری نمونه، استخراج و پیش تغلیظ
اسید استیک در آماده سازی نمونه زمانی مفید است که اسیدی کردن ملایم باعث بهبود پایداری، بازده استخراج، یا انتخاب پذیری تحلیلی شود. در پژوهش های محیط زیست و غذا، اسیدی کردن کنترل شده می تواند فعالیت زیستی را کاهش دهد، برخی فرایندهای تخریب را کند کند، و آنالیت ها را در شکل شیمیایی مناسب تر در طول نگهداری و انتقال حفظ کند. در روش های استخراج، تنظیم pH با اسید استیک می تواند رفتار تقسیم در استخراج مایع مایع را تغییر دهد، اتصال در استخراج فاز جامد را بهتر کند، یا به مراحل پاکسازی که تداخل های بازی را حذف می کند کمک کند. در برخی مفاهیم استخراج مرحله ای، اسیدهای ملایم برای هدف گیری بخش های قابل آزادسازی تر یک ماتریس پیچیده استفاده می شوند و این کار به مطالعه ی نحوه ی اتصال یا آزاد شدن اجزا کمک می کند. در تحلیل متابولیت ها و مولکول های کوچک، گاهی اسید استیک برای اسیدی کردن فازهای آبی انتخاب می شود در حالی که سازگاری با جداسازی و آشکارسازی بعدی حفظ می شود. چون آماده سازی نمونه منبع اصلی تغییرپذیری است، آزمایشگاه ها غلظت، زمان تماس، و سازگاری ظرف را استاندارد می کنند و این پارامترها را در SOP و گزارش روش ثبت می کنند. این کار اسید استیک را به یک ابزار تکرارپذیری در مسیرهای پیچیده ی پژوهش دانشگاهی تبدیل می کند.
ایمنی، کاربری و مدیریت ریسک اسید استیک
ایمنی در کاربرد اسید استیک در آزمایشگاه و پژوهش دانشگاهی به این بستگی دارد که پژوهشگر بداند غلظت چگونه ریسک را تغییر می دهد و سپس کنترل مناسب را با کار تطبیق دهد. اسید استیک غلیظ خورنده است، می تواند سوختگی شدید پوست و چشم ایجاد کند، و بخار آن راه های تنفسی را تحریک می کند؛ بنابراین کار معمول با آن بهتر است در هود شیمیایی و با عینک ایمنی، دستکش مقاوم، و روپوش انجام شود. چون اختلاط گرما تولید می کند، رقیق سازی باید با تکنیک منظم و افزودن آهسته همراه با همزدن انجام شود تا نقاط داغ و پاشش شدید ایجاد نشود. نگهداری باید با جداسازی از مواد ناسازگار مثل اکسید کننده های قوی و بازهای واکنش پذیر انجام گیرد و درپوش ها باید محکم بسته باشند تا بخار کمتر آزاد شود. برنامه ی مدیریت ریزش نیز در فضاهای آموزشی و پژوهشی ضروری است: ریزش های کوچک با ابزار مناسب قابل مهار و خنثی سازی است، اما ریزش های بزرگ به روش های رسمی و افراد آموزش دیده نیاز دارد. آمادگی کمک های اولیه هم مهم است و شستشوی فوری با آب و پیگیری پزشکی در صورت تداوم علائم باید انجام شود. فرهنگ برچسب گذاری، آموزش، و SOP های مستند باعث می شود اسید استیک مفید بماند و آشنایی روزمره به حادثه ی قابل پیشگیری تبدیل نشود.
| کار یا سناریو | شکل یا غلظت معمول | ریسک اصلی | کنترل های کلیدی | واکنش سریع اگر مشکل پیش آمد |
|---|---|---|---|---|
| برداشتن از بطری محلول مادر | گلاسیال یا غلیظ | استنشاق بخار، سوختگی | هود، عینک، دستکش سازگار | رفتن به هوای تازه، شستشوی پوست با آب |
| رقیق سازی تا محلول کاری | غلیظ تا 0.1 تا 10 درصد | گرما، پاشش | افزودن آهسته، همزدن، شیلد | شستشوی چشم یا پوست با آب، گزارش مواجهه |
| اسیدی کردن فاز متحرک | 0.1 تا 1 درصد حجمی | تحریک، ناسازگاری با دستگاه | گرید مناسب، تیوب سازگار | توقف پمپ، شستشوی سیستم، تهویه |
| مرحله اسیدی در بافت شناسی | 0.5 تا 5 درصد | پاشش، بخار | ظرف درب دار، تهویه موضعی | شستشو فوری، تعویض PPE آلوده |
| پشتیبانی از مراحل اسید نوکلئیک | سامانه استات، اسید ملایم | آسیب نمونه در اضافه کردن زیاد | قطره ای افزودن، کنترل pH | خنثی سازی با احتیاط، تکرار آماده سازی |
| تنظیم محیط کشت سلول | بسیار رقیق | شوک pH موضعی | پیش رقیق سازی، اختلاط کامل | دور ریختن محیط مشکل دار، ثبت انحراف |
| رسوب زدایی شیشه آلات یا قطعات | 1 تا 10 درصد | پاشش، انتقال باقی مانده | سینی ثانویه، آبکشی کامل | خنثی سازی پسماند، آبکشی چندباره |
| پاکسازی ریزش در کلاس آموزشی | متغیر | سوختگی تماس، بخار | کیت ریزش، PPE، محدود کردن فضا | مهار، خنثی سازی در صورت آموزش، ارجاع در صورت تردید |




