فهرست عناوین
- مقدمه ای بر اسیدهای آلی و اهمیت آن ها در شیمی
- ساختار مولکولی اسید استیک : بررسی گروه کاربکسیل
- تفاوت های ساختاری اسید استیک و سایر اسیدهای آلی
- تفاوت در ویژگی های اسیدی بین اسید استیک و سایر اسیدهای آلی
- خصوصیات فیزیکی اسید استیک در مقایسه با اسیدهای آلی دیگر
- گروه های جانبی در اسید استیک و اثر آن ها بر ساختار
- تفاوت در واکنش های شیمیایی اسید استیک و سایر اسیدهای آلی
- اسید استیک در برابر اسید فرمیک : تفاوت های ساختاری و کاربردها
- اسید سیتریک و اسید استیک : تفاوت در ساختار و کاربردهای بیولوژیکی
- تفاوت در تأثیر گروه های مختلف کاربکسیل در اسیدهای آلی
- تفاوت های ساختاری اسید استیک با اسیدهای هیدروکسی کربوکسیلیک
نوشته شده توسط شرکت صنایع استیک ایران
منتشر شده توسط شرکت صنایع استیک ایران
تاریخ انتشار مقاله : 26-11-1403
تاریخ بروزرسانی مقاله : 26-11-1403
تعداد کلمات : 1700
آدرس مقاله : لینک مقاله
تفاوت ساختار اسید استیک با سایر اسیدهای آلی
مقدمه ای بر اسیدهای آلی و اهمیت آن ها در شیمی
اسیدهای آلی ترکیبات آلی هستند که حاوی یک یا چند گروه عاملی کربوکسیل (-COOH) می باشند. که در ادامه به بررسی فرمول مولکولی اسید استیک (CH3COOH) و خواص آن خواهیم پرداخت. این گروه عامل اسیدی بودن این ترکیبات است. اسیدهای آلی در طبیعت به صورت گسترده وجود دارند و نقش های حیاتی در متابولیسم جانداران ایفا می کنند. سیتریک اسید در مرکبات ، لاکتیک اسید در شیر ترشیده و استیک اسید در سرکه نمونه هایی از این اسیدها هستند. کاربردهای اسیدهای آلی در صنایع بسیار متنوع است. در صنعت غذا به عنوان طعم دهنده و نگهدارنده ، در تولید داروها ، پلاستیک ها ، رنگ ها و حلال ها از آن ها استفاده می شود. اسید استیک ساده ترین اسید کربوکسیلیک از اهمیت ویژه ای برخوردار است. این ترکیب به طور گسترده در صنایع مختلف از تولید سرکه تا تولید پلیمرها کاربرد دارد و درک ساختار و ویژگی های آن برای درک شیمی اسیدهای آلی ضروری است.
ساختار مولکولی اسید استیک : بررسی گروه کاربکسیل
اسید استیک (CH₃COOH) ساده ترین اسید کربوکسیلیک است. ساختار آن شامل یک گروه متیل (CH₃) متصل به یک گروه کربوکسیل (-COOH) است. گروه کربوکسیل از یک گروه کربونیل (C=O) و یک گروه هیدروکسیل (-OH) تشکیل شده است. پیوند هیدروژنی بین مولکول های اسید استیک نقطه جوش نسبتا بالای آن را توجیه می کند. گروه کربوکسیل نقش اساسی در ویژگی های شیمیایی اسید استیک ایفا می کند. اتم هیدروژن گروه هیدروکسیل به راحتی یونیزه می شود و یون استات (CH₃COO⁻) و یک پروتون (H⁺) را تولید می کند. این خاصیت اسیدی اسید استیک را قادر می سازد تا با بازها واکنش داده و نمک های استات را تشکیل دهد. واکنش پذیری گروه کربونیل در سنتز استرها و آمیدها نیز نقش مهمی دارد. تفاوت در زنجیره کربنی متصل به گروه کربوکسیل منجر به تفاوت در ویژگی های اسیدهای آلی مختلف می شود.
| ویژگی | توضیحات | ساختار مولکولی | قطبیت و حلالیت | فعالیت شیمیایی | ویژگیهای پیوندی |
|---|---|---|---|---|---|
| فرمول شیمیایی | CH3COOH | ساختار خمیده به دلیل جاذبههای الکترونی | مولکول قطبی به دلیل حضور گروه -COOH | واکنش با بازها برای تشکیل استات | پیوند دوگانه C=O در گروه کربوکسیل |
| ساختار لوییس | دارای یک گروه کربوکسیل (-COOH) متصل به گروه متیل | اتم اکسیژن دارای جفت الکترونهای آزاد | محلول در آب و سایر حلالهای قطبی | تشکیل استرها در حضور الکل | پیوند هیدروژنی بین مولکولهای اسید استیک |
| زاویه پیوند | حدود 120 درجه در گروه کربوکسیل | دارای هیبریداسیون sp2 در گروه کربوکسیل | میتواند در اتانول و متانول حل شود | قابلیت شرکت در واکنشهای افزایشی و جانشینی | زاویه خمیدگی در گروه کربوکسیل |
| قطبیت | قطبی به دلیل گروه کربوکسیل | تشکیل پیوند هیدروژنی قوی با مولکولهای آب | حلالیت کاهش مییابد در حلالهای غیرقطبی | واکنش با فلزات برای تشکیل استات فلزی | پیوند کووالانسی قوی بین اتمهای کربن و اکسیژن |
| نوع پیوند | پیوندهای کووالانسی، پیوند هیدروژنی در محلول آبی | پیوند دوگانه کربن-اکسیژن در گروه کربوکسیل | تشکیل پیوندهای هیدروژنی با مولکولهای آب | اکسایش پذیر در شرایط خاص | ساختار رزونانسی پایدار در گروه کربوکسیل |
| فعالیت شیمیایی | اسیدیته متوسط، توانایی تشکیل استرها و آمیدها | قابلیت تبدیل به یون استات در محلول آبی | قابلیت جذب آب از هوا (جاذب رطوبت) | فعال در واکنشهای تراکمی | تأثیر پیوند هیدروژنی بر نقطه جوش بالا |
| کاربردهای خاص | استفاده در تولید پلاستیک، مواد غذایی، و داروسازی | استفاده در واکنشهای اسیدی-بازی | استفاده به عنوان حلال در صنایع مختلف | استفاده در تولید مواد شیمیایی صنعتی | تجمع مولکولی در فاز مایع به دلیل پیوند هیدروژنی |
تفاوت های ساختاری اسید استیک و سایر اسیدهای آلی
اسید استیک (CH₃COOH) ساده ترین اسید کربوکسیلیک با دو اتم کربن است. اسید فرمیک (HCOOH) کوتاه ترین عضو این خانواده با تنها یک اتم کربن است. در مقابل اسید بوتریک (CH₃CH₂CH₂COOH) چهار اتم کربن در زنجیره آلکیل خود دارد. اسید سیتریک (C₆H₈O₇) ساختاری پیچیده تر با سه گروه کربوکسیل و یک گروه هیدروکسیل دارد. این تفاوت در طول زنجیره کربنی و وجود گروه های عاملی دیگر ساختار و ویژگی های این اسیدها را به طور قابل توجهی متمایز می کند. اسید استیک زنجیره آلکیلی کوتاه و خطی دارد درحالی که اسید بوتریک زنجیره بلندتری دارد و اسید سیتریک ساختار شاخه دار و چند عاملی دارد. وجود شاخه ها و گروه های عاملی دیگر مانند هیدروکسیل بر پایداری و واکنش پذیری اسید تأثیر می گذارد. این اختلافات ساختاری موجب تفاوت در خواص فیزیکی و شیمیایی مانند نقطه جوش ، حلالیت و واکنش پذیری می شود.
تفاوت در ویژگی های اسیدی بین اسید استیک و سایر اسیدهای آلی
قدرت اسیدی یک اسید کربوکسیلیک به تمایل آن برای آزادسازی یون هیدروژن (H⁺) بستگی دارد که تحت تأثیر اثر القایی و رزونانس گروه های آلکیل و عاملی دیگر قرار می گیرد. اسید استیک قدرت اسیدی متوسطی دارد. اسید فرمیک فاقد گروه آلکیل قدرت اسیدی بیشتری از اسید استیک نشان می دهد زیرا گروه های آلکیل الکترون دهنده هستند و آزادسازی پروتون را دشوار می کنند. اسیدهای با زنجیره آلکیل بلندتر مانند اسید بوتریک قدرت اسیدی ضعیف تری نسبت به اسید استیک دارند. اسید سیتریک با سه گروه کربوکسیل قدرت اسیدی بیشتری از اسید استیک دارد. سه گروه کربوکسیل به طور همزمان در پایداری یون سیترات نقش دارند و گروه های هیدروکسیل آن از طریق پیوند هیدروژنی ، پایداری این یون را افزایش می دهند. بنابراین قدرت اسیدی اسیدهای کربوکسیلیک به طول زنجیره آلکیل ، تعداد گروه های کربوکسیل و سایر گروه های عاملی موجود در ساختار مولکولی آن ها بستگی دارد. هر چه اثر الکترون کشنده گروه های عاملی بیشتر باشد قدرت اسیدی بیشتر است.
خصوصیات فیزیکی اسید استیک در مقایسه با اسیدهای آلی دیگر
اسید استیک مایعی بی رنگ با بوی تند و مشخص است. نقطه جوش آن 118 درجه سانتیگراد است که نسبت به اسید فرمیک با نقطه جوش 101 درجه سانتیگراد بالاتر است. این تفاوت به دلیل افزایش جرم مولکولی و افزایش نیروهای بین مولکولی در اسید استیک است. اسیدهای با زنجیره آلکیل بلندتر نقطه جوش بالاتری دارند. برای مثال اسید بوتانوئیک نقطه جوش 164 درجه سانتیگراد دارد. حلالیت اسید استیک در آب بسیار بالاست و به راحتی با آب مخلوط می شود. این به دلیل توانایی تشکیل پیوند هیدروژنی با مولکول های آب است. اسیدهای آلی با زنجیره آلکیل بلندتر حلالیت کمتری در آب دارند. چگالی اسید استیک 1.05 گرم بر سانتی متر مکعب است که کمی بالاتر از چگالی آب است. این خصوصیات فیزیکی اسید استیک نتیجه مستقیم ساختار مولکولی آن و نیروهای بین مولکولی است که بین مولکول های آن وجود دارد.
گروه های جانبی در اسید استیک و اثر آن ها بر ساختار
اسید استیک دارای یک گروه متیل (CH₃) به عنوان گروه جانبی است که به گروه کربوکسیل (-COOH) متصل است. این گروه متیل اثر القایی الکترون دهنده دارد. یعنی الکترون ها را به سمت گروه کربوکسیل می راند و میزان بار منفی روی اکسیژن ها را افزایش می دهد. این اثر قدرت اسیدی اسید استیک را نسبت به اسید فرمیک (که فاقد گروه آلکیل است) کاهش می دهد. در اسیدهای آلی دیگر طول و ساختار زنجیره آلکیل تاثیر قابل توجهی بر خواص فیزیکی و شیمیایی آن ها دارد. اسیدهای با زنجیره آلکیل بلندتر قدرت اسیدی کمتری نشان می دهند. وجود شاخه ها در زنجیره آلکیل نیز بر قدرت اسیدی اثر می گذارد. علاوه بر گروه های آلکیل وجود گروه های عاملی دیگر مانند هالوژن ها ، گروه های هیدروکسیل یا گروه های آمینو باعث تغییرات قابل توجهی در ساختار و خواص اسید می شود. این گروه ها با اثر القایی یا رزونانس خود قدرت اسیدی را افزایش یا کاهش می دهند.
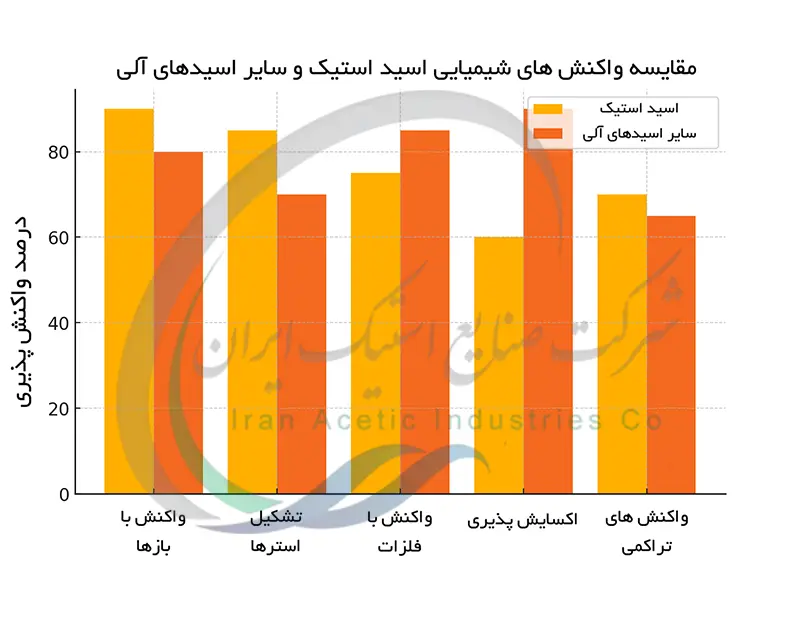
تفاوت در واکنش های شیمیایی اسید استیک و سایر اسیدهای آلی
اسید استیک مانند دیگر اسیدهای کربوکسیلیک در واکنش های استری شدن ، هیدرولیز و اکسایش شرکت می کند. با این حال سرعت و بازده این واکنش ها به ساختار اسید بستگی دارد. در استری شدن اسید استیک با الکل ها واکنش داده و استر تولید می کند. سرعت این واکنش به دلیل گروه متیل کوچک آن نسبتاً بالا است. هیدرولیز استرهای استات نیز به آسانی انجام می شود. اکسایش اسید استیک به دی اکسید کربن و آب رخ می دهد ولی این واکنش نسبت به اکسایش اسیدهای آلی دیگر با زنجیره های کربنی بلندتر ، آهسته تر است. اسیدهای آلی با زنجیره های کربنی بلندتر واکنش های جانبی بیشتری از خود نشان می دهند و محصولات متنوعی تولید می کنند. اکسایش اسیدهای چرب پیچیده تر است و باعث تولید کتون ها یا اسیدهای دیکربوکسیلیک می شود.
اسید استیک در برابر اسید فرمیک : تفاوت های ساختاری و کاربردها
اسید استیک و اسید فرمیک ساده ترین اسیدهای کربوکسیلیک هستند. اسید استیک یک گروه متیل به گروه کربوکسیل متصل دارد در حالی که اسید فرمیک فاقد این گروه است. اسید استیک نقطه جوش بالاتری دارد و قدرت اسیدی ضعیف تری نسبت به اسید فرمیک نشان می دهد. این به دلیل اثر القایی الکترون دهنده گروه متیل است که تراکم بار منفی روی اکسیژن کربوکسیل را افزایش می دهد و در نتیجه تمایل به از دست دادن پروتون کاهش می یابد. اسید استیک به طور گسترده در تولید سرکه ، پلیمرها و حلال ها استفاده می شود. اسید فرمیک کاربردهایی در صنایع نساجی ، دباغی چرم و به عنوان یک ماده ضدعفونی کننده دارد. اسید استیک به دلیل پایداری بیشتر و هزینه پایین تر کاربرد وسیع تری دارد.
اسید سیتریک و اسید استیک : تفاوت در ساختار و کاربردهای بیولوژیکی
اسید استیک ساده ترین اسید کربوکسیلیک با یک گروه کربوکسیل است در حالی که اسید سیتریک ساختاری پیچیده تر با سه گروه کربوکسیل و یک گروه هیدروکسیل دارد. این تفاوت ساختاری کاربردهای بیولوژیکی متفاوتی را برای آن ها رقم می زند. اسید استیک در بسیاری از فرآیندهای متابولیکی نقش دارد و در تنظیم PH بدن دخیل است. اسید سیتریک عنصری کلیدی در چرخه کربس ، مسیر مرکزی تولید انرژی در سلول های زنده می باشد. در صنایع غذایی اسید استیک به عنوان طعم دهنده و نگهدارنده استفاده می شود در حالی که اسید سیتریک در نوشیدنی ها ، مواد غذایی و به عنوان عامل طعم دهنده و تنظیم کننده PH کاربرد دارد. خاصیت آنتی اکسیدانی اسید سیتریک نیز در صنایع غذایی و دارویی مورد توجه قرار میگیرد.
تفاوت در تأثیر گروه های مختلف کاربکسیل در اسیدهای آلی
اسید استیک یک گروه کربوکسیل دارد. اسیدهای چرب یک گروه کربوکسیل در انتهای زنجیره هیدروکربنی خود دارند. طول زنجیره و اشباع یا غیر اشباع بودن آنها بر خواص شیمیایی و فیزیکی اسید چرب اثر می گذارد. اسیدهای آمینه یک گروه کربوکسیل و یک گروه آمینو دارند. موقعیت نسبی این دو گروه و گروه های جانبی متنوع آن ها خواص اسیدهای آمینه را بسیار متنوع می کند. در اسید استیک تأثیر گروه کربوکسیل بر ویژگی های اسیدی و واکنش پذیری مشخص است. در اسیدهای چرب اثر گروه کربوکسیل همراه با اثر زنجیره هیدروکربنی بررسی می شود. در اسیدهای آمینه وجود گروه آمینو و گروه های جانبی علاوه بر گروه کربوکسیل نقش تعیین کننده ای در خواص آن ها دارد.
تفاوت های ساختاری اسید استیک با اسیدهای هیدروکسی کربوکسیلیک
اسید استیک یک اسید کربوکسیلیک ساده با تنها یک گروه کربوکسیل است. اسیدهای هیدروکسیکربوکسیلیک مانند اسید لاکتیک علاوه بر گروه کربوکسیل دارای یک یا چند گروه هیدروکسیل (-OH) نیز هستند. این گروه هیدروکسیل به طور مستقیم به زنجیره کربنی متصل به گروه کربوکسیل وصل است. وجود گروه هیدروکسیل بر خواص اسیدی حلالیت و واکنش پذیری این اسیدها تاثیر می گذارد. پیوند هیدروژنی بین گروه هیدروکسیل و گروه کربوکسیل یا مولکول های آب باعث افزایش حلالیت اسیدهای هیدروکسیکربوکسیلیک نسبت به اسید استیک می شود. همچنین گروه هیدروکسیل بر قدرت اسیدی نیز اثر می گذارد. در اسید لاکتیک گروه هیدروکسیل مجاور گروه کربوکسیل با ایجاد اثر القایی و تشکیل پیوند هیدروژنی داخلی قدرت اسیدی را کمی کاهش می دهد. این تفاوت های ساختاری باعث کاربردهای متفاوت این دو نوع اسید در صنایع مختلف می شود.




