فهرست عناوین
نوشته شده توسط شرکت صنایع استیک ایران
منتشر شده توسط شرکت صنایع استیک ایران
تاریخ انتشار مقاله : 12-05-1404
تاریخ بروزرسانی مقاله : 12-05-1404
تعداد کلمات : 2200
آدرس مقاله : لینک مقاله
مقایسه راندمان روش های بیولوژیکی و شیمیایی تولید اسید استیک

مقدمه
خرید اسید استیک فناوران گالن 20 لیتری که یک ماده شیمیایی بسیار مهم است ، در صنایع مختلف از نگهداری مواد غذایی گرفته تا ساخت پلاستیک ها کاربرد دارد. این ماده به دو روش زیستی (تخمیری) یا سنتز شیمیایی قابل تولید است. هر روش مزایا و محدودیت های خاص خود را دارند. در حال حاضر بخش اعظم تولید صنعتی اسید استیک از طریق روش های شیمیایی انجام می شود. از سوی دیگر تخمیر زیستی عمدتا برای تولید سرکه اهمیت خود را حفظ کرده است ، زیرا قوانین مواد غذایی در بسیاری کشورها ایجاب می کند سرکه مصرفی منشا زیستی داشته باشد.
روش های تولید زیستی اسید استیک
تخمیر باکتریایی یک روش شناخته شده برای تولید اسید استیک است و به ویژه در تهیه سرکه خوراکی کاربرد دارد. در این فرایند زیستی(بیولوژیکی) میکروب ها (مثلا گونه های باکتری استوباکتر) اتانول را به اسید استیک اکسید می کنند. در روش های سنتی تولید سرکه از تکنیک هایی مانند روش اورلئان یا فرآیند ژنراتور قطره ای استفاده می شود که فرآیندهای بچ یا نیمه پیوسته بوده و تکمیل آنها چندین هفته طول می کشد. در تولید صنعتی مدرن سرکه معمولا از فرآیند تخمیر غوطه ور در مخازن ویژه تخمیر (اسیتاتور) استفاده می شود تا فرآیند اسیدسازی سریع تر انجام گیرد. مسیر زیستی محلول نسبتا رقیقی از اسید استیک (سرکه با غلظت معمولا ۵ تا ۱۵٪) حاصل می شود و معمولا اگر اسید خالص نیاز باشد به فرآوری بیشتری برای تغلیظ احتیاج دارد. با این حال این روش ذاتا کندتر و کم بازده تر نسبت روش شیمیایی برای تولید در مقیاس بزرگ است.
روش های تولید شیمیایی اسید استیک
کربونیلاسیون متانول مهم ترین روش صنعتی تولید اسید استیک است و بیشترین سهم تولید جهانی را به خود اختصاص می دهد. در این فرایند (مانند فرایند مونسانتو و کاتیوا) ، متانول در حضور یک کاتالیزور (معمولا کمپلکس رودیوم یا ایریدیوم) با گاز مونوکسید کربن واکنش داده و اسید استیک تولید می شود. این مسیر شیمیایی بسیار کارآمد است و به صورت پیوسته تحت دما و فشار بالا عمل می کند و اسید استیک با خلوص بالا (گلاسیال) تولید می کند. فرایندهای شیمیایی دیگری نیز (مانند اکسایش استالدهید یا بوتان) برای تولید اسید استیک وجود دارند ، اما امروزه به دلیل کارایی پایین تر چندان متداول نیستند و عمدتا با فناوری کربونیلاسیون متانول جایگزین شده اند.
مواد اولیه و خوراک
تولید زیستی اسید استیک متکی بر خوراک های آلی تجدیدپذیر است که بررسی مواد اولیه قابل استفاده در تخمیر اسید استیک از اهمیت بالایی برخوردار است. در تخمیر سرکه معمولا از اتانول حاصل از محصولات کشاورزی (مثلا شراب انگور ، سایدر سیب یا الکل غلات) به عنوان ماده اولیه استفاده می شود و باکتری های اسید استیک آن را به اسید استیک اکسید می کنند. برخی فرایندها می توانند قندها یا نشاسته ها را به طور مستقیم به اسید استیک تخمیر کنند ، اگرچه معمولا ابتدا باید قند به اتانول تبدیل شود. همچنین فناوری های زیستی نوظهور حتی از زیست توده پسماند استفاده کرده یا گاز سنتز (CO + H2) را توسط میکروب های ویژه به اسید استیک تبدیل می کنند که دامنه مواد اولیه تجدیدپذیر را گسترش می دهد. در مقابل تولید شیمیایی اسید استیک وابسته به مواد اولیه پتروشیمی (فسیلی) است. متانولی که در فرایند کربونیلاسیون استفاده می شود معمولا از گاز طبیعی (از طریق گاز سنتز) تولید می شود. مسیرهای شیمیایی دیگری نیز در گذشته از واسطه های مشتق از فسیل مانند استالدهید (از اتیلن) یا هیدروکربن های سبک (مثل بوتان) استفاده می کردند که با اکسایش به اسید استیک تبدیل می شوند. در مجموع مسیر زیستی می تواند از خوراک های تجدیدپذیر استفاده کند در حالی که مسیر شیمیایی متکی بر مواد اولیه غیرقابل تجدید مبتنی بر سوخت فسیلی است.
شرایط عملیاتی و نیازهای انرژی
یکی از تفاوت های عمده بین این دو مسیر تولید در شرایط عملیاتی و نیازهای انرژی آنها است. تخمیر در شرایط ملایمی انجام می شود : معمولا در دمای حدود ۲۵ تا ۳۷ درجه سانتیگراد (نزدیک به دمای محیط) و فشار اتمسفری. باکتری های اسید استیک به اکسیژن نیاز دارند (برای تخمیر هوازی) و همچنین کنترل دقیق pH و استریل بودن محیط برای جلوگیری از آلودگی ضروری است. انرژی مورد نیاز در طول تخمیر نسبتا پایین است زیرا این فرآیند به گرمایش شدید یا فشار بالا نیاز ندارد ؛ البته مقداری انرژی برای هم زدن محیط کشت و پمپاژ هوا به منظور هوادهی مصرف می شود. در مقابل سنتز شیمیایی اسید استیک (مثلا کربونیلاسیون متانول) تحت شرایط به مراتب سخت تری انجام می شود. راکتورها در دماهای بالا (حدود ۱۵۰ تا ۲۰۰ درجه سانتیگراد) و فشارهای زیاد با گاز CO تحت فشار در حضور کاتالیزور عمل می کنند. انرژی قابل توجهی برای گرم کردن مخلوط واکنش و حفظ این فشار بالا لازم است. تجهیزات باید به گونه ای طراحی شوند که در برابر مواد شیمیایی خورنده و فشار زیاد مقاومت کنند که این امر پیچیدگی فرایند را افزایش می دهد. اگرچه فرآیند شیمیایی در مرحله واکنش انرژی بیشتری مصرف می کند ، اما محصول غلیظ تری تولید می کند که جداسازی نهایی را آسان تر می سازد. در مقابل فرآیند زیستی در طول واکنش انرژی کمتری مصرف می کند ولی در ادامه برای تقطیر محصول رقیق به انرژی قابل توجهی نیاز دارد.
بازده تبدیل و کارایی
بازده تبدیل یکی از شاخص های اصلی کارایی است که نشان می دهد چه مقدار از ماده اولیه به اسید استیک تبدیل می شود. فرآیندهای زیستی نسبت به خوراک مستقیم خود می توانند بازده بالایی داشته باشند اما ممکن است به تبدیل تقریبا کامل که در فرآیندهای شیمیایی مشاهده می شود نرسند. به عنوان مثال در تخمیر سرکه که اتانول به عنوان خوراک استفاده می شود ، تبدیل اتانول به اسید استیک می تواند حدود ۹۰ تا ۹۵٪ حداکثر نظری برسد. مقداری اتلاف نیز رخ می دهد زیرا بخشی از ماده اولیه صرف رشد میکروبی می شود یا به محصولات جانبی مانند CO2 ، به ویژه اگر شکر خوراک اولیه باشد تبدیل می گردد. در مقابل فرآیند کربونیلاسیون متانول در تولید شیمیایی معمولا بیش از ۹۵٪ بازده تولید اسید استیک از متانول را به دست می دهد و محصولات جانبی بسیار کمی تولید می شود. در عملیات صنعتی سنتز شیمیایی می تواند تقریبا تمام خوراک را به اسید استیک تبدیل کند ، در حالی که بازده تخمیر هرچند بالا اندکی کمتر و متغیرتر است.
نرخ و زمان تولید
نرخ تولید نیز حوزه دیگری است که در آن روش های زیستی و شیمیایی تفاوت چشمگیری دارند. فرآیندهای تخمیر ذاتا کندتر هستند ، زیرا محدود به رشد و متابولیسم میکروبی می باشند. حتی در سامانه های بهینه شده تخمیر سرکه ، تولید یک بچ اسید استیک ممکن است ساعت ها تا روزها طول بکشد. روش های سنتی مانند فرآیند اورلئان به چندین هفته زمان نیاز داشتند تا شراب را به طور کامل به سرکه تبدیل کنند. تخمیرکننده های صنعتی مدرن با بهبود تأمین اکسیژن و استفاده از باکتری های پربازده این زمان را به یک یا دو روز برای هر بچ کاهش داده اند. با این وجود بهره وری حجمی تولید (بر حسب گرم اسید استیک تولید شده در لیتر در ساعت) در تخمیر همچنان در مقایسه با فرآیندهای شیمیایی نسبتا پایین است. از سوی دیگر تولید شیمیایی می تواند با سرعت بسیار بیشتری اسید استیک تولید کند. در راکتورهای پیوسته کربونیلاسیون متانول ، خوراک به طور مداوم به محصول تبدیل می شود و این امکان را می دهد که یک کارخانه واحد صدها یا هزاران تن اسید استیک در روز تولید کند. سرعت واکنش بالا است و کارکرد پیوسته به این معناست که مانند تخمیر وقفه ای بین بچ ها وجود ندارد. در نتیجه روش شیمیایی توان تولیدی بسیار بالاتری نسبت به هر فرآیند تخمیر زیستی دارد. یک کارخانه شیمیایی می تواند تقاضای در مقیاس بزرگ را به سرعت پاسخ دهد در حالی که یک فرآیند زیستی برای تولید همان میزان اسید استیک به زمان بسیار بیشتر و حجم راکتورهای بزرگ تر نیاز خواهد داشت.
مقیاس پذیری و تولید صنعتی
قابلیت مقیاس پذیری یکی از ملاحظات حیاتی در تولید صنعتی است. روش های تخمیر زیستی به صورت ذاتی محدودیت هایی در زمینه مقیاس دارند. مخازن تخمیر تنها تا اندازه مشخصی می توانند بزرگ ساخته شوند ، زیرا محدودیت هایی در انتقال اکسیژن ، دفع گرما و خطر آلودگی وجود دارد. برای تولید حجم بسیار زیادی اسید استیک از طریق تخمیر به تعداد زیادی تخمیرکننده موازی و زمان قابل توجهی نیاز خواهد بود. تقاضای جهانی برای اسید استیک (میلیون ها تن در سال) با فناوری فعلی به تنهایی از طریق تخمیر قابل تامین نیست. در عمل تولید سرکه با تخمیر در مقیاس نسبتا کوچکی انجام می شود (در حد نیاز صنایع غذایی) ، اما به سطح مقیاس مورد نیاز بازارهای عمده مواد شیمیایی گسترش نیافته است. در مقابل روش های تولید شیمیایی به شدت مقیاس پذیر هستند. کارخانه های صنعتی اسید استیک که از کربونیلاسیون متانول بهره می برند می توانند طوری طراحی شوند که صدها هزار تا بیش از یک میلیون تن در سال را در یک واحد تولید کنند. این فرآیندها به صورت پیوسته اجرا می شوند و می توان با استفاده از راکتورهای بزرگ تر یا خطوط تولید متعدد آنها را مقیاس بندی کرد. قابلیت مقیاس پذیری مسیر شیمیایی به این معناست که می تواند به سادگی حجم عظیم اسید استیک مورد نیاز صنایعی مانند تولید پلاستیک را تامین کند. بنابراین از دیدگاه امکان پذیری صنعتی ، روش های شیمیایی به مراتب توانمندتر از روش های زیستی در تولید اسید استیک در مقیاس بزرگ هستند.
خلوص محصول و فرآوری نهایی
تخمیر زیستی اسید استیک را به صورت یک محلول آبی رقیق تولید می کند. در تخمیر معمول سرکه غلظت اسید استیک تولیدی تنها حدود ۵ تا ۱۵٪ است (بقیه آن آب و متابولیت های فرعی است). برای مصارف خوراکی مانند سرکه ، این محصول رقیق قابل قبول بوده و به صورت مستقیم یا با حداقل فیلتراسیون استفاده می شود. اما اگر قرار باشد اسید استیک غلیظ یا خالص از محیط تخمیر به دست آید ، به عملیات فرآوری گسترده پس از تخمیر نیاز خواهد بود. این محلول رقیق باید تقطیر شود تا آب حذف شده و اسید استیک تغلیظ گردد. تقطیر اسید استیک از نظر انرژی بسیار پرهزینه است زیرا حاوی مقدار زیادی آب است و نقطه جوش آن نسبتا بالا است. در نتیجه تولید اسید استیک گلاسیال (تقریبا ۱۰۰٪ خالص) از طریق تخمیر به لحاظ اقتصادی چالش برانگیز است. در مقابل تولید شیمیایی اسید استیک را به شکل بسیار غلیظ تری حاصل می کند. در فرآیند کربونیلاسیون متانول ، مخلوط واکنش حاوی بخش عمده ای اسید استیک به همراه مقادیر کمی محصولات جانبی و آب است. فرآیندهای صنعتی شامل مراحل جداسازی (مثل برج های تقطیر) برای خالص سازی اسید استیک هستند ، اما از آنجا که غلظت اولیه محصول نسبتا بالا است ، دستیابی به اسید استیک خالص آسان تر بوده و انرژی کمتری مصرف می کند. نتیجه این می شود که اسید استیک گلاسیال (با خلوص معمولا بیش از ۹۹٪) مستقیما از فرآیند شیمیایی به دست می آید. این محصول با خلوص بالا برای کاربردهای صنعتی ایده آل است. نمودار پایین مقایسه ای از خلوص محصول نهایی و موفقیت فرآوری (تصفیه و خالص سازی) در دو روش تولید اسید استیک (زیستی و شیمیایی) را نشان می دهد.
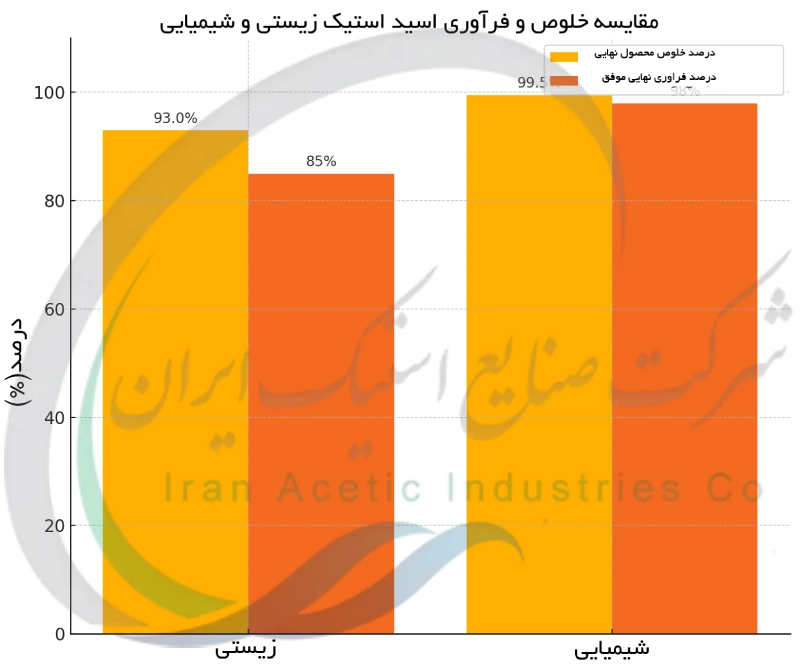
مقایسه کارایی روش های زیستی و شیمیایی
پس از بررسی هر جنبه توليد ، روشن است كه هر يك از روش های شيميايی و زيستی نقاط قوت و ضعف خاص خود را دارند. از نظر كارايی ذاتی (بازده و نرخ توليد) ، سنتز شيميايی از تخمير پيشی می گيرد. خوراك را به شكل كامل تری به اسيد استيك تبديل میكند و با سرعت بسيار بالاتری آن را توليد می كند. فرآيندهای شيميايی همچنين به راحتی مقياس پذير هستند و محصولی با غلظت بالا توليد می كنند. از سوی ديگر تخمير زيستی تحت شرايط ملايم تری انجام می شود و می تواند از منابع تجديدپذير بهره ببرد ، كه علی رغم بهره وری پايين تر به آن مزيت زيست محیطی می دهد. از نظر هزينه ، مقياس بزرگ و كارايی مسير شيميايی آن را برای توليد انبوه اقتصادی تر می سازد ، در حالی كه مسير زيستی هزينه بيشتری به ازای هر واحد اسيد توليد شده دارد. جدول زير مقايسه ای تطبيقی از پارامترهای كليدی كارايی بين روش های توليد زيستی (تخمیری) و شيميايی (سنتزی) اسيد استيك ارائه می دهد. در اين جدول نشان داده شده است كه هر كدام از اين دو رویکرد در زمينه هايی مانند بازده ، سرعت ، مصرف انرژی ، مقياس پذيری ، كيفيت محصول و پايداری در چه جايگاهی قرار دارند:
| معیار | زیستی (تخمیری) | شیمیایی (سنتزی) | مزیت | توضیحات |
|---|---|---|---|---|
| بازده (کارایی تبدیل) | بالا (تا ~۹۰٪) اما میتواند با خوراک شکر کمتر باشد | بسیار بالا (~۹۵–۹۹٪) | شیمیایی | مسیر شیمیایی تقریباً تمام خوراک را به محصول تبدیل میکند |
| نرخ تولید | کند (نیازمند ساعتها تا روزها) | سریع (تولید پیوسته) | شیمیایی | تخمیر محدود به متابولیسم میکروبی است، در حالی که راکتورهای شیمیایی با سرعت بالایی اسید استیک تولید میکنند |
| شرایط عملیاتی | ملایم (دما ~۳۰°C، فشار اتمسفری) | سخت (دما ~۱۸۰°C، فشار بالا) | زیستی | تخمیر در شرایط ملایم انجام میشود؛ سنتز شیمیایی به شرایط سخت و تجهیزات ویژه نیاز دارد |
| مصرف انرژی | کم در واکنش؛ زیاد برای جداسازی محصول (تقطیر آب) | زیاد در واکنش؛ متوسط در جداسازی | متغیر | فرآیند زیستی در مرحله واکنش انرژی کمتری مصرف میکند ولی برای بازیابی محصول به انرژی زیادی نیاز دارد، بنابراین مصرف کلی انرژی تقریباً مشابه است |
| مقیاسپذیری | محدود – مقیاس کردن به حجمهای بسیار بزرگ دشوار است | بسیار بالا – کارخانههای بزرگ میلیونها تن تولید میکنند | شیمیایی | فرآیند شیمیایی بهراحتی برای تأمین تقاضای جهانی مقیاس میپذیرد، در حالی که تخمیر از نظر مقیاس محدودیت دارد |
| غلظت محصول | رقیق (سرکه ۵–۱۵٪ اسید استیک) | غلیظ (اسید استیک گلاسیال ~۹۹٪ خلوص) | شیمیایی | روش شیمیایی مستقیماً اسید استیک تقریباً خالص تولید میکند؛ تخمیر یک اسید رقیق میدهد که نیاز به تغلیظ دارد |
| هزینه هر واحد | بالاتر (خوراک گرانتر و فرآیند پرهزینهتر) | پایینتر (خوراک ارزان و فرآیند کارا) | شیمیایی | تولید اسید استیک تخمیری پرهزینهتر است؛ اسید استیک شیمیایی در مقیاس صنعتی ارزانتر تمام میشود |
| تأثیر زیستمحیطی | پتانسیل تقریباً کربنخنثی (استفاده از زیستتوده؛ سوخت فسیلی کمتر) | متکی بر سوخت فسیلی (ردپای کربنی قابل توجه) | زیستی | مسیر زیستی با خوراک تجدیدپذیر پایدارتر است، در حالی که مسیر شیمیایی گازهای گلخانهای بیشتری منتشر میکند |




